附加项目(说明)
以下是临诊小组作业的额外附加部分。(因本站将会永久维护运营,故本条说明将在本学期结束后删除)
关于甲状腺异常导致的疾病症状及机制
甲状腺功能亢进常引起心律失常,而心律失常往往又会引起心绞痛、心肌梗死甚至心力衰竭。然而,这些心脏病变的最根本原因是过量甲状腺激素对心肌代谢、血流动力学及神经内分泌(如交感 - 肾上腺髓质系统、肾素 - 血管紧张素 - 醛固酮系统)的不利影响。因此,甲状腺功能亢进是疾病的主导环节,治疗时应针对甲状腺功能亢进。可见,了解疾病发展的主导环节,对诊断和治疗疾病具有重要意义。
高渗性脱水:
高热、大量出汗和甲状腺功能亢进时,均可通过皮肤丢失大量低渗液体从而引起高渗性脱水。
水电解质代谢紊乱:
甲状腺功能亢进时,甲状腺激素可抑制肾小管重吸收镁。甲状腺激素还具有溶骨作用,中度甲亢患者约 20% 伴高钙血症。甲状腺功能减退时,甲状腺激素合成和分泌减少,其抑制肾小管重吸收镁作用减弱,肾排镁障碍。
呼吸性碱中毒:
甲状腺功能亢进时,机体代谢旺盛,由于血液温度过高和机体分解代谢亢进可刺激引起呼吸中枢兴奋,通气过度使 PaCO2 降低。
糖脂代谢紊乱:
甲状腺功能减退时,甲状腺激素水平直接影响脂质代谢的各个环节,LDLR 活性和 LPL 活性降低,脂代谢紊乱主要表现为高胆固醇血症及高甘油三酯血症等。同时,甲状腺激素增多时,能诱导肝 HMG - CoAR 表达增加,胆固醇合成增加。
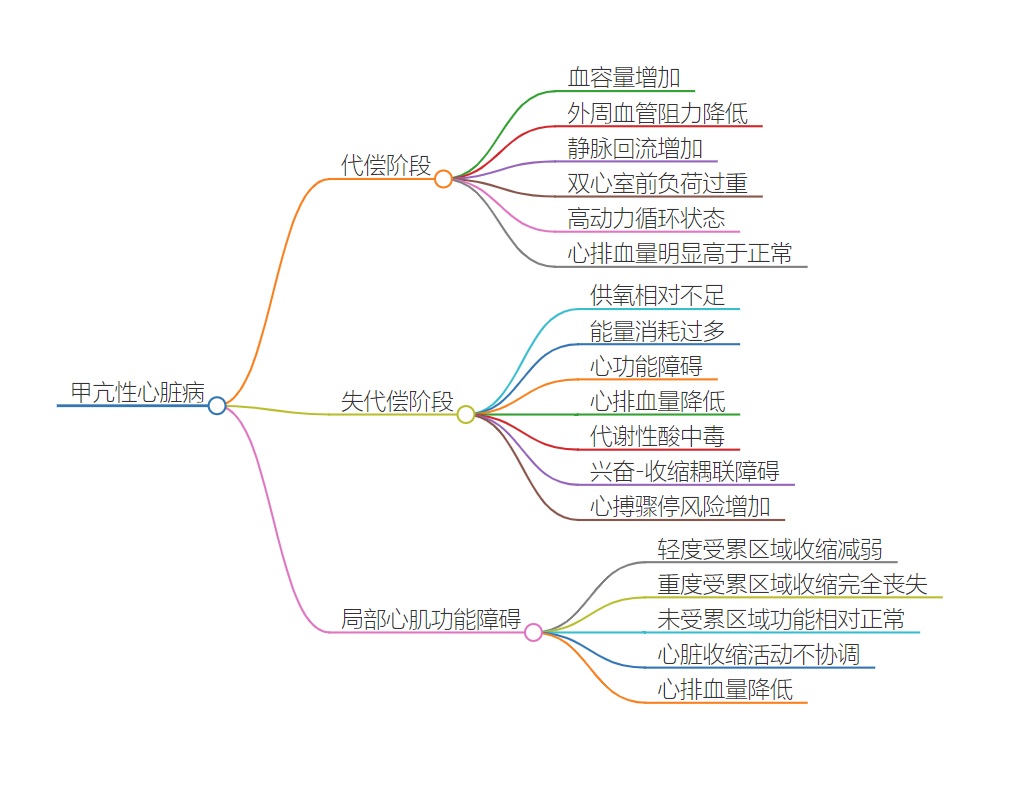
心功能不全:
甲亢时回心血量增加,左、右心室前负荷都过重。外周血管阻力降低,血容量扩大或循环速度加快,静脉回流增加,心脏过度充盈,代偿阶段其心排血量明显高于正常,处于高动力循环状态,即在全身代偿和心脏代偿共同作用下,机体稳态得以维持。由于心脏容量负荷长期过重,供氧相对不足,能量消耗过多,一旦发展至心功能不全失代偿阶段,心排血量较心功能不全代偿阶段有所下降,不能满足上述病因造成的机体高水平代谢的需求,但患者的心排血量仍高于或不低于正常群体的平均水平。临床上,由于心功能失代偿阶段机体代谢性酸中毒,乳酸缓慢升高,导致心肌细胞兴奋 - 收缩耦联障碍,易突发心搏骤停,危及生命。同时,由于病变呈区域性分布,病变轻的区域心肌舒缩活动减弱,病变重的心肌完全丧失收缩功能,非病变心肌功能相对正常,甚至代偿性增强,整个心脏的舒缩活动不协调,导致心排血量下降。
甲状腺肿瘤癌症相关症状与机制
1. 甲状腺乳头状癌(PTC)引发的症状和机制
- 症状/体征:颈部淋巴结转移(15%患者)、肿瘤生长缓慢但局部侵袭性增加。
机制:
- BRAF突变:BRAF V600E突变通过激活MAPK信号通路,导致肿瘤细胞增殖、侵袭和血管生成增加[1]。
- RET/PTC重排:RET/PTC基因融合激活RAS/MAPK和PI3K/AKT信号通路,增强肿瘤侵袭性。
- NTKR1基因重排:少数患者(<5%)染色体重排激活NTKR1,导致受体酪氨酸激酶活性异常,增强细胞增殖和存活。
2. 甲状腺滤泡癌(FTC)引发的症状和机制
- 症状/体征:肿瘤侵袭血管和囊膜,易发生远处转移(如肺和骨)。
机制:
- RAS突变:RAS激活PI3K/AKT通路,促进细胞生长和存活。
- PAX8-PPARγ易位:导致融合蛋白表达异常,干扰甲状腺特异基因的正常调控,促进癌变。
- PTEN失活:PI3K/AKT信号通路过度激活,抑制细胞凋亡,支持肿瘤存活)。
3. 间变性甲状腺癌(ATC)引发的症状和机制
- 症状/体征:快速生长的肿块,侵袭周围器官(如气管、食管),表现为呼吸困难、吞咽困难,并伴随疼痛。
机制:
- TP53突变:失活的TP53导致细胞失去调控DNA修复、细胞周期和凋亡的功能,促使肿瘤去分化[1], [4]。
- TERT启动子突变:通过延长端粒,支持肿瘤细胞无限增殖[1], [4]。
- 多个信号通路激活:MAPK、PI3K/AKT、Wnt/β-Catenin等共同作用,促进侵袭和耐药性[1], [2], [4]。
4. 女性甲状腺癌(TC)的高发症状和机制
- 症状/体征:女性甲状腺癌发病率显著高于男性,尤其在育龄期;可能伴随肿瘤侵袭性增加。
机制:
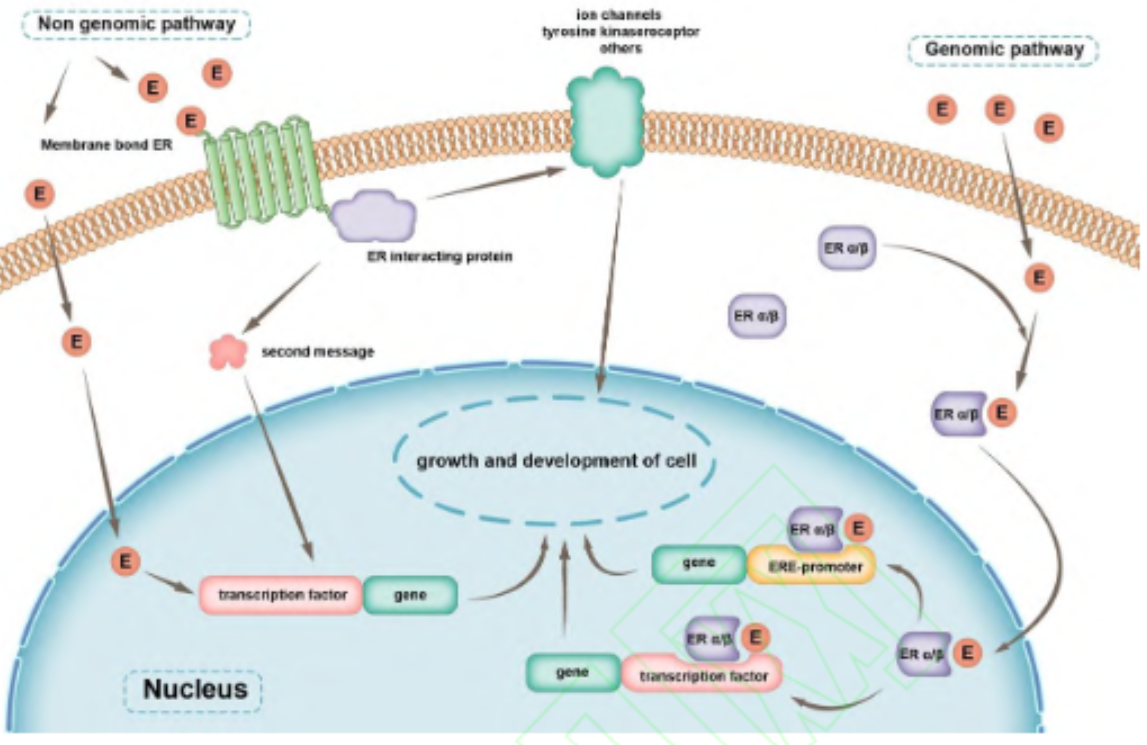
- 雌激素作用:
- ERE基因途径:雌激素与ER(尤其是ERα)结合后激活ERE通路,促进RET/PTC重排、下游信号通路磷酸化和肿瘤细胞增殖([5])。
- 非基因途径:通过GPR30受体快速激活细胞内信号通路,刺激甲状腺细胞生长[5]。
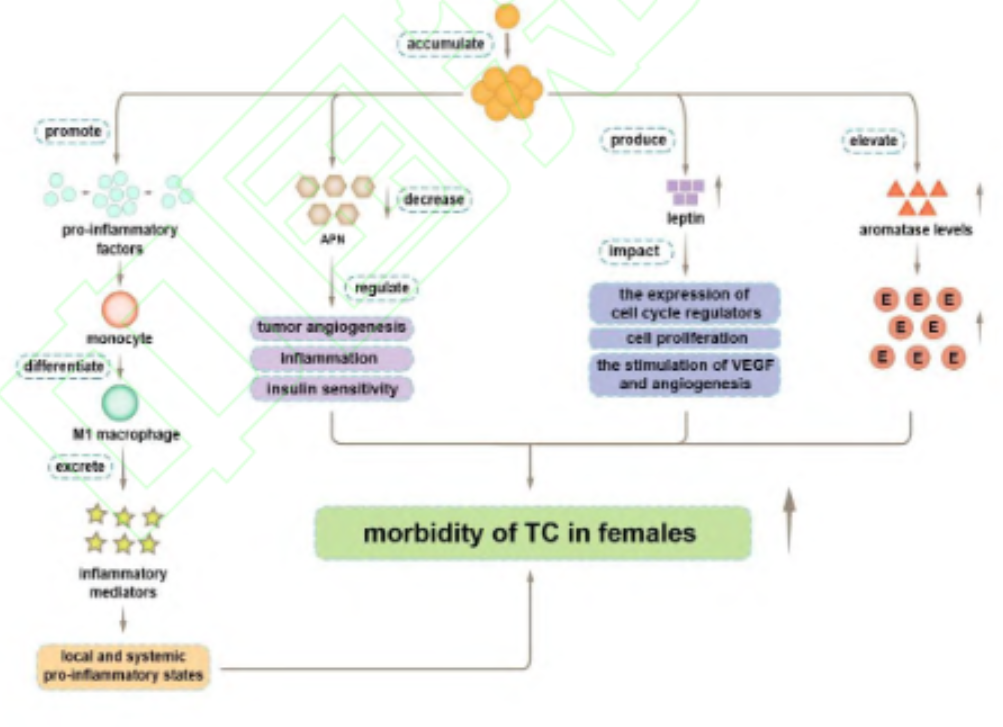
- 肥胖相关机制:
- 脂肪组织分泌瘦素、芳香化酶,增加雌激素水平,进一步促进肿瘤生长[5]。
- 促炎因子释放,形成促癌性微环境[5]。
- X染色体基因差异:部分X染色体基因逃脱失活,导致女性肿瘤易感性增加[5]。
5. 甲状腺结节(TN)引发的症状和机制
- 症状/体征:
- 低回声信号、结节内血流丰富(恶性TN特征)。
- 部分患者出现局部压迫症状(如吞咽困难或声音嘶哑)。
机制:
- TSH刺激:促甲状腺激素过度刺激甲状腺细胞生长,导致结节形成。
- RET/PTC重排:部分恶性结节中激活MAPK通路,促进细胞增殖。
- 氧化-抗氧化失衡:H2O2过量积累导致DNA损伤和RET/PTC重排,诱发肿瘤[5]。
其他相关症状与机制
1. 术后相关症状和机制
- 症状/体征:
- 血清T3、T4波动,部分患者出现甲状腺功能减退。
- 颈部异样感觉或神经损伤导致长期不适。
- 术后结节触感变硬。
机制:
- 激素波动:术后甲状腺激素释放紊乱,可能由术中甲状腺组织灭活释放激素引起[2]。
- 组织脱水:微波消融或射频治疗导致组织水分丢失,使结节变硬[2]。
- 神经损伤:手术切断颈部末梢神经,导致长期异样感觉[2]。
2. 甲状腺癌信号通路异常引发的症状和机制
- 症状/体征:肿瘤侵袭性增加,淋巴结转移,远处转移(如肺、骨)。
机制:
- MAPK信号通路:由BRAF、RAS突变或RET/PTC重排激活,引起肿瘤细胞增殖、迁移和血管生成[1], [2]。
- PI3K/AKT信号通路:PTEN失活或PI3K突变导致信号通路过度活跃,支持肿瘤存活、侵袭和耐药性[1], [3]。
- Wnt/β-Catenin信号通路:RET突变或PI3K/AKT异常激活β-Catenin,推动肿瘤去分化和侵袭[1]。
- NF-κB信号通路:通过调控炎症因子和凋亡基因,促进肿瘤侵袭和转移[2]。
3. 特殊机制:氧化-抗氧化系统失衡
- 症状/体征:甲状腺肿瘤细胞DNA损伤、RET/PTC重排增加。
机制:
- H2O2生成过量:在女性甲状腺细胞中,H2O2酶活性下降导致氧化物积累,进而增加DNA损伤和癌变风险[5]。
4. 分娩和生殖相关症状与机制
- 症状/体征:分娩期女性甲状腺癌风险增加,部分患者肿瘤侵袭性增强。
机制:
- hCG作用:妊娠期人绒毛膜促性腺激素(hCG)刺激TSH和ER,增加肿瘤细胞增殖和侵袭能力[5]。
- 雌激素水平升高:ER通路激活,诱导肿瘤相关基因表达[5]。
参考文献
- 陈里新, 张奇, 李涵阳, 等. 甲状腺癌遗传学研究进展. 吉林医学, 2016, 37(07): 1777-1779.
- 陈宝定, 赵双双, 陈延玮, 等. 未分化甲状腺癌分子机制和治疗进展. 江苏大学学报(医学版), 2021, 31(02): 93-100.
- 彭琛. PTPRE激活AKT/FOXO1和ERK/c-Myc信号通路促进甲状腺癌进展的机制研究. 山西医科大学, 2023.
- 谭美娟, 杨诗婕, 刘真钻, 等. 女性甲状腺癌高发的病因研究进展. 协和医学杂志, 2024.
- 黄钦海. 广佛接壤地区社区女性甲状腺结节的临床特征及相关危险因素研究. 广州医科大学, 2020.